نظرة عامة
يصف مرض الرئة الخلالي، ويُعرف أيضًا باختصار ILD، مجموعة كبيرة من الحالات المرضية. تتسبب معظم هذه الحالات في حدوث التهاب وتندب تدريجي لأنسجة الرئة. وكجزء من هذه العملية، تزداد سماكة أنسجة الرئة وتصلبها، ما يجعل من الصعب على الرئتين التمدد والامتلاء بالهواء.
في مرحلة ما، يؤدي التندّب الناجم عن مرض الرئة الخلالي إلى صعوبة التنفس وإدخال كمية كافية من الأكسجين إلى مجرى الدم. ويصاب العديد من الأشخاص المصابين بمرض الرئة الخلالي بضيق في التنفس عند بذل مجهود، بينما يصاب البعض الآخر بسعال جاف مزعج.
يمكن أن يكون لمرض الرئة الخلالي العديد من الأسباب، بما في ذلك التعرض الطويل الأمد للمخلفات الخطرة مثل الأسبستوس. كما يمكن أن تسبب بعض أنواع أمراض المناعة الذاتية، مثل التهاب المفاصل الروماتويدي، مرض الرئة الخلالي. ولكن في بعض الأحيان لا يكون السبب معروفًا. يمكن أن يكون لمرض الرئة الخلالي العديد من الأسباب، لذلك يختلف العلاج.
قد يزداد المرض سوءًا ببطء أو بسرعة بوتيرة لا يمكن التنبؤ بها غالبًا. بمجرد حدوث تندب الرئة، لا يمكن علاج هذه الحالة بشكل عام. يركز العلاج على منع حدوث المزيد من التندّبات، والتحكم في الأعراض وتحسين جودة الحياة. قد تبطئ الأدوية من تلف مرض الرئة الخلالي، لكن العديد من الأشخاص لا تستعيد رئتاهم وظيفتها بشكل كامل مرة أخرى. زرع الرئة هو خيار لبعض الأشخاص المصابين بمرض الرئة الخلالي.
المنتجات والخدمات
الأعراض
الأعراض الرئيسية لمرض الرئة الخلالي هي:
- ضيق التنفس أثناء الراحة أو ضيق التنفس الذي يزداد سوءًا مع ممارسة الأنشطة البدنية.
- السعال الجاف.
الحالات التي تستلزم زيارة الطبيب
بحلول الوقت الذي تظهر فيه الأعراض في أنواع معينة من مرض الرئة الخلالي، يكون قد حدث بالفعل تلف دائم في الرئة. ولذلك من المهم زيارة اختصاصي الرعاية الصحية عند ظهور أول مؤشر على وجود مشكلات في التنفس. يمكن أن تؤثر العديد من الحالات الأخرى غير مرض الرئة الخلالي في الرئة. من المهم الحصول على تشخيص مبكر ودقيق للحصول على العلاج المناسب.
الأسباب
القُصيبات والحويصلات داخل الرئتين
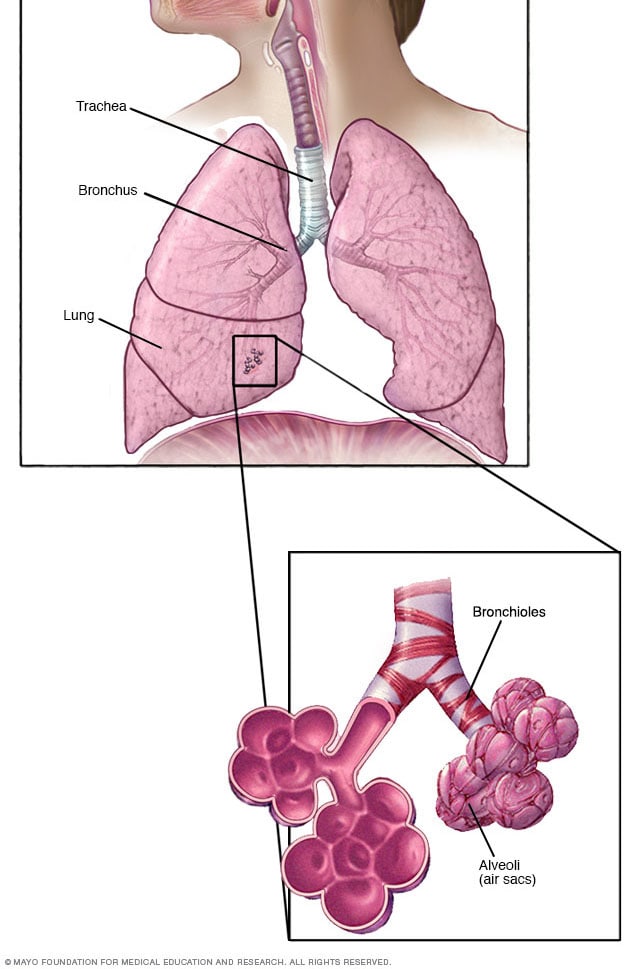
القُصيبات والحويصلات داخل الرئتين
داخل الرئتين، يتفرع الممران الهوائيان الرئيسيان، يسميان القصبتين الهوائيتين، إلى ممرات أصغر وأصغر.
وتُسمى أصغرها بالقُصيبات، وتوجد في نهايتها أكياس هوائية صغيرة تسمى الحويصلات.
يبدو أن مرض الرئة الخلالي يحدث عندما تتسبب إصابة في الرئة في استجابة غير مناسبة للشفاء. في الظروف الطبيعية، يُنتج الجسم الكمية الصحيحة من النسيج لإصلاح التضرر. ولكن في مرض الرئة الخلالي، لا تحدث عملية الإصلاح بشكل صحيح. تصبح الأنسجة داخل الأكياس الهوائية في الرئتين وحولها، والتي تُسمى الحويصلات الهوائية، ملتهبة ومتندبة وسميكة. وهذا يجعل من الصعب مرور الأكسجين إلى مجرى الدم.
هناك العديد من أنواع مرض الرئة الخلالي. وعادةً ما تُصنف بناءً على الأسباب المعروفة أو غير المعروفة:
- العمل أو البيئة المحيطة.
- حالة صحية كامنة مجموعية.
- أنواع معينة من الأدوية أو الإشعاع.
- دون سبب معروف.
يمكن أن تكون بعض أمراض الرئة الخلالية مرتبطة بالتدخين.
العمل أو البيئة المحيطة
يؤدي التعرض لبعض السموم والملوثات لفترات طويلة إلى تلف الرئتين. على سبيل المثال:
- تغبر الرئة. يشير تغبر الرئة إلى أحد أنواع مرض الرئة الخلالي الناجمة عن استنشاق أنواع معينة من الغبار في العمل أو بيئات أخرى لفترة طويلة. قد تؤدي أمراض هذه المجموعة إلى تندّب الرئة وإصابتها بمرور الوقت، ما يؤدي إلى ضيق النفس وضعف القدرة على استنشاق الأكسجين. ومن غير الممكن الرجوع إلى وضع ما قبل هذه الأعراض. غالبًا ما يُسمى المرض نسبةً إلى نوع التعرض أو طبيعة العمل نفسه. ومن هذه الأمراض رئة مُعدِّني الفحم الناجمة عن استنشاق غبار الفحم، وداء الأَسبست الناجم عن استنشاق جسيمات الأسبست. وتتضمن هذه الأمراض أيضًا سحار سيليسي الناجم عن استنشاق غبار السيليكا.
- الالتهاب الرئوي الناتج عن فرط التحسس. ينجم هذا الالتهاب الرئوي عن استنشاق المهيجات المنقولة بالهواء، التي غالبًا ما تتضمن بروتينات الكائنات الحية. ومن أكثر هذه المهيجات المنقولة بالهواء شيوعًا بروتين الطيور أو العفن أو البكتيريا. غالبًا ما تُسمى الحالات من هذا النوع أيضًا باسم نوع التعرض أو مصدره. على سبيل المثال، ينجم مرض رئة مُربِّي الحمام أو محبي الطيور عن التعرض لبروتين الطيور، وينجم مرض رئة المزارع عن التعرض للقش المتعفن. يمكن للأشخاص المصابين بهذا النوع من التهاب الرئة أن يتحسنوا من خلال الابتعاد عن المهيجات. لكن هذا النوع من التهاب الرئة يمكن أن يزداد سوءًا ويؤدي إلى أضرار تدوم طويلاً إذا استمر الأشخاص في استنشاق المادة المهيجة.
الحالة الصحية الكامنة المَجموعية
قد تؤدي بعض الأمراض أو الحالات إلى مرض الرئة الخلالي. على سبيل المثال:
- أمراض الأنسجة الضامة. تتضمن هذه الأمراض أمراض المناعة الذاتية، مثل التهاب المفاصل الروماتويدي وتصلب الجلد ومرض النسيج الضام المختلط. تؤدي هذه الأمراض إلى استجابة مناعية غير سليمة وقد تسبب التهاب الأنسجة وتندّبًا في الجسم، بما في ذلك الرئتان.
- الساركويد. وهو مرض يحدث فيه نمو غير طبيعي لتجمعات صغيرة من الخلايا الالتهابية تُسمى الأورام الحُبيبية في أي جزء من الجسم، وفي معظم الحالات يصيب الرئتين والعُقَد اللمفية. تشمل الأعضاء الأخرى المصابة عادةً العينين والجلد والقلب والطحال والكبد.
الأدوية والإشعاع
يمكن أن تؤدي أنواع معينة من الأدوية إلى إصابة بعض الأشخاص بمرض الرئة الخلالي. وقد تكون هذه الحالة قابلة للعلاج أو غير قابلة للعلاج بناءً على نوع التعرض ومدته.
الأدوية الأكثر ارتباطًا بمرض الرئة الخلالي:
- أدوية العلاج الكيميائي. يمكن للأدوية المصممة لقتل الخلايا السرطانية أن تلحق الضرر بأنسجة الرئة، ومن هذه الأدوية بليوميسين وجيمسيتابين ومثبطات نقاط التفتيش المناعية.
- أدوية القلب. بعض الأدوية المستخدمة في علاج اضطراب نبض القلب، مثل الأميودارون (Nexterone وPacerone)، يمكن أن تَضر أنسجة الرئة.
- بعض المضادات الحيوية. يمكن أن يؤدي نتروفورانتوين (Macrobid وMacrodantin وغيرهما) ودابتوميسين إلى تلف الرئة.
- الأدوية المضادة للالتهاب. يمكن لبعض الأدوية المضادة للالتهابات، مثل ميثوتريكسات (Trexall وXatmep وغيرهما) أو سلفاسالازين (Azulfidine)، أن تلحق الضرر بالرئتين.
قد يؤدي الإشعاع الموجه إلى الصدر أثناء علاج أنواع معينة من السرطانات، مثل سرطان الثدي وسرطان الرئة، إلى تعرض بعض الأشخاص لإصابة أو ندبات طويلة الأمد. وقد تعتمد مدى خطورة التضرر على:
- حجم جزء الرئة الذي تعرض للإشعاع.
- إجمالي كمية الإشعاع المُستخدمة.
- ما إذا كان استُخدِم العلاج الكيميائي أيضًا.
- ما إذا كان الشخص مصابًا بمرض كامن في الرئة.
لا يوجد سبب معروف
قائمة المواد والحالات التي يمكن أن تؤدي إلى مرض الرئة الخلالي طويلة. ومع ذلك، لا يُعرف سببه عند بعض الأشخاص مطلقًا. تُجمع الحالات التي ليس لها سبب معروف تحت مسمى التهاب الرئة الخلالي مجهول السبب. على سبيل المثال:
- التليف الرئوي مجهول السبب (IPF). التليف الرئوي مجهول السبب مرض رئوي متفاقم بطبيعته يحدث عندما تتلف أنسجة الرئة وتتندب، وهو ما يُعرف بالتليف. ويُقصد بمجهول السبب أن سببه غير معروف. يمكن رؤية التليف الرئوي مجهول السبب في التصوير والخزعة إذا أُخذت خزعة من الرئة. يمنع هذا النسيج السميك والصلب الرئتين من العمل بشكل سليم. التليف الرئوي مجهول السبب هو النوع الأكثر شيوعًا من أمراض الرئة الخلالية، وغالبًا ما يتفاقم ولا يمكن علاجه.
- التهاب الرئة المنظم خفي المنشأ (COP). التهاب الرئة المنظم خفي المنشأ حالة رئوية نادرة تلتهب فيها المجاري الهوائية الصغيرة، التي تُسمى القصيبات، وأكياس تبادل الهواء الصغيرة، التي تُسمى الحويصلات الهوائية. يجعل هذا الالتهاب التنفُّس صعبًا. تُظهر الاختبارات التصويرية وجود التهاب رئوي، لكن التهاب الرئة المنظم خفي المنشأ ليس عَدوى، وسببه غير معروف. التندّب أو التليف نادر الحدوث، لكنه قد يحدث لدى بعض المرضى إذا عادت الحالة مرة أخرى.
- التهاب الرئة الخلالي غير النوعي. يؤدي هذا النوع من أمراض الرئة الخلالية إلى التهاب الخلايا أو تراكم النسيج الندبي في الفراغات بين الأكياس الهوائية في الرئتين. ومن المرجح أن يحدث لدى الأشخاص المصابين بأمراض النسيج الضام، لكن يمكن أن يكون مرتبطًا أيضًا بحالات أخرى.
عوامل الخطر
تشمل العوامل التي قد تجعل المريض أكثر عرضة للإصابة بمرض الرئة الخلالي ما يلي:
- العمر. من المرجح بشكل كبير أن يؤثر مرض الرئة الخلالي في البالغين، رغم أن الأطفال والرضع قد يصابون بالمرض في بعض الأحيان.
- التعرض للسموم في العمل أو البيئة. العمل في التعدين أو الزراعة أو البناء، أو التعرض لأي ملوثات معروفة بتلف الرئتين، يزيد من خطر الإصابة بمرض الرئة الخلالي.
- التدخين. من المرجح أن تحدث بعض أشكال مرض الرئة الخلالي لدى الأشخاص الذين لديهم سيرة مَرضية من التدخين. قد يزيد التدخين النشط من سوء الحالة، ولا سيما إذا كنت مصابًا أيضًا بالنفاخ الرئوي.
- المعالجات الإشعاعية والكيميائية. وجود علاجات إشعاعية للصدر، أو استخدام بعض أدوية المعالجة الكيميائية يمكن أن يزيد من خطر الإصابة بأمراض الرئة.
- أمراض الأنسجة الضامة. يشمل ذلك أمراض المناعة الذاتية التي يمكن أن تزيد من خطر الإصابة بمرض الرئة الخلالي.
المضاعفات
يمكن أن يؤدي مرض الرئة الخلالي إلى سلسلة من المضاعفات المهددة للحياة، بما في ذلك:
- ارتفاع ضغط الدم في الرئتين ويُسمى أيضًا بارتفاع ضغط الدم الرئوي. على عكس ارتفاع ضغط الدم المَجموعي، تؤثر هذه الحالة في الشرايين الموجودة في الرئة فقط. تقيد الأنسجة الندبية أو انخفاض مستويات الأكسجين أصغر الأوعية الدموية، ما يحد من تدفق الدم في الرئة. وهذا يرفع الضغط داخل الشرايين الرئوية ويمكن أن يؤدي إلى تفاقم تبادل الأكسجين، ما يقلل من مستويات الأكسجين في الدم. إن ارتفاع ضغط الدم الرئوي مرضًا خطيرًا قد يزداد سوءًا مع مرور الوقت، ما يتسبب في فشل الجانب الأيمن من القلب.
- فشل الجانب الأيمن من القلب، والمعروف أيضًا باسم القصور الرئوي الأيمن. تحدث هذه الحالة الخطيرة عندما يتعين على الحجرة اليمنى السفلية للقلب والمعروفة أيضًا باسم البطين الأيمن ضخ الدم بقوة أكبر من المعتاد لنقل الدم عبر الشرايين الرئوية المسدودة. وفي نهاية المطاف، يفشل البطين الأيمن بسبب الضغط الإضافي. وغالبًا ما يرجع ذلك إلى ارتفاع ضغط الدم الرئوي.
- الفشل التنفسي. تحدث الإصابة بالفشل التنفسي في المرحلة الأخيرة من مرض الرئة الخلالي المزمن عندما تتسبب مستويات الأكسجين في الدم المنخفضة بشدة، إلى جانب ارتفاع الضغط في الشرايين الرئوية والبطين الأيمن، في فشل القلب.
الوقاية
للوقاية من مرض الرئة الخلالي، تجنَّب التعرض للسموم في العمل، مثل الأسبستوس وغبار الفحم وغبار السيليكا. تجنَّب أيضًا التعرض للسموم الموجودة في البيئة، مثل بروتين الطيور والعفن والبكتيريا. إذا كان لا بد من الوجود حول هذه السموم، فاحرص على حماية نفسك بارتداء جهاز تنفس. تشمل الطرق الأخرى للوقاية من الإصابة بمرض الرئة الخلالي عدم التدخين وتجنب التدخين السلبي.
إذا كنت مصابًا بأحد أمراض المناعة الذاتية أو كنت تتناول أدوية تزيد من خطر الإصابة بمرض الرئة الخلالي، فتحدث إلى اختصاصي الرعاية الصحية بشأن الخطوات التي يمكنك اتخاذها للوقاية من الإصابة بمرض الرئة الخلالي. احرص أيضًا على تلقي اللقاحات لأن العَدوى التنفسية يمكن أن تفاقم أعراض مرض الرئة الخلالي. وتأكد من حصولك على لقاح التهاب الرئة ومطعوم الإنفلونزا كل عام. اسأل أيضًا اختصاصي الرعاية الصحية عن الحصول على لقاح السعال الديكي وكوفيد 19 والفيروس المخلوي التنفسي (RSV).