概述
阿尔茨海默病是失智最常见的病因。阿尔茨海默病是一个生理过程,最开始显示为淀粉样斑块形式的蛋白和神经原纤维缠结在脑中的积聚。这导致脑细胞随时间推移而死亡以及脑部萎缩。
在美国,大约有 690 万 65 岁及以上的人患有阿尔茨海默病。其中,超过 70% 为 75 岁及以上的人。在全球超过 5500 万失智患者中,估计 60% 至 70% 患有阿尔茨海默病。
阿尔茨海默病的早期症状包括忘记最近发生的事情或对话。随时间推移,阿尔茨海默病会导致严重的记忆丧失,并影响一个人完成日常任务的能力。
阿尔茨海默病无法治愈,在晚期阶段,脑功能丧失可能会导致脱水、营养不良或感染。这些并发症可能导致死亡。
但药物可能改善症状或减缓思维衰退。有各种项目和服务可以为该病患者及其照护者提供支持。
症状
记忆丧失是阿尔茨海默病的主要症状。在疾病早期,患者可能难以记住最近发生的事情或谈话内容。随着时间的推移,记忆力会越来越差,并出现其他症状。
起初,患者可能会意识到自己难以记住事情和清晰思考。随着症状和体征的加重,家人或朋友可能更容易注意到这些问题。
阿尔茨海默病引起的脑部变化会导致以下症状随着时间的推移而加重。
记忆力
每个人有时都会出现记忆问题,但与阿尔茨海默病相关的记忆丧失是持久的。随着时间的推移,记忆丧失会影响您在工作和家庭中发挥功能的能力。
阿尔茨海默病患者可能:
- 不断重复同一句话或同一个问题。
- 忘记谈话、预约或事件。
- 把物品放错地方,经常把物品放在不合适的地方。
- 在他们曾经熟悉的地方迷路。
- 忘记家人姓名和日常物品的名称。
- 难以找到恰当的词语、表达想法或进行交谈。
思考与推理
阿尔茨海默病会导致难以集中注意力和思考,尤其是对像数字这样的抽象概念。同时做多项任务尤其困难。管理财务、计算开支和按时支付账单可能具有挑战性。最终,阿尔茨海默病患者可能无法识别数字。
做出判断和决定
阿尔茨海默病会让人很难做出明智的决定和判断。阿尔茨海默病患者可能在社交场合做出有失明智的举动,或者穿着不合时令的衣物。日常问题可能难以解决。阿尔茨海默病患者可能不知道如何处理炉子上烧焦的食物,也不知道如何在开车时做出决定。
计划和执行熟悉的任务
对于需要遵循特定顺序完成步骤的常规活动,阿尔茨海默病患者可能也难以完成。他们可能难以制定计划和做饭或玩喜欢的游戏。阿尔茨海默病进展至晚期后,患者会忘记如何完成穿衣和浸浴等基本任务。
性格和行为发生变化
阿尔茨海默病导致的脑部变化会影响情绪和行为。症状可能包括:
- 抑郁。
- 对活动失去兴趣。
- 社交退缩。
- 情绪波动。
- 不信任他人。
- 愤怒或攻击性。
- 睡眠习惯发生变化。
- 游荡。
- 丧失自制力。
- 妄想,例如认为有东西被偷了(其实并没被偷)。
保留的技能
尽管阿尔茨海默病患者的记忆力和技能会发生重大变化,但即使症状加重,他们仍能保留一些技能。这些被称为保留技能,可能包括阅读或听书、讲故事和分享回忆、唱歌、听音乐、跳舞、绘画或做手工。
保留技能之所以能保留更长时间,是因为管理这些技能的脑部分在疾病晚期才会受到影响。
何时就诊
有几种状况可能会导致记忆丧失或其他失智症状。其中有些状况是可以治疗的。如果您对自己的记忆力或其他思维能力感到担忧,请咨询医疗护理专业人员。
如果您对在家人或朋友身上观察到的思维能力感到担忧,可以询问是否可以一起去咨询医疗护理专业人员。
病因
健康大脑和阿尔茨海默病患者的大脑
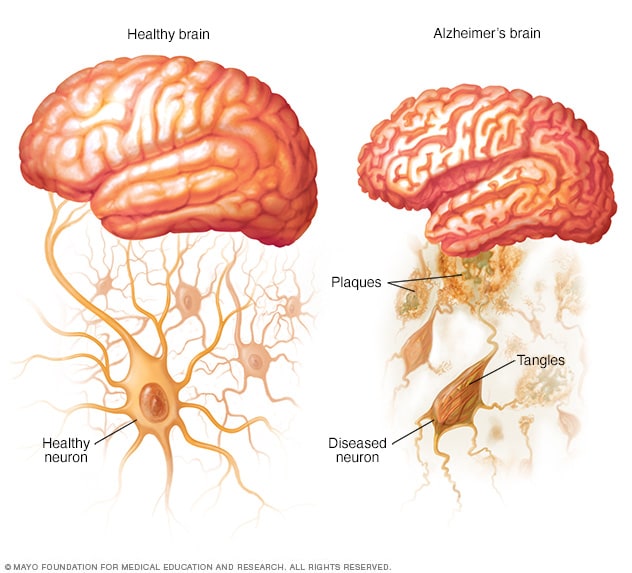
健康大脑和阿尔茨海默病患者的大脑
阿尔茨海默病患者的大脑中会形成淀粉样斑块,Tau 蛋白形状改变,并相互缠结。
阿尔茨海默病的确切病因尚不完全清楚。但从根本上说,大脑蛋白质失去正常功能。这扰乱了脑细胞(也称为神经元)的工作,进而引发一系列事件。神经元受损,失去相互连接,最终神经元死亡。
科学家认为,对于大多数患者,阿尔茨海默病是遗传、生活方式和环境因素共同作用的结果,这些因素会随着时间的推移对大脑产生影响。只有不到 1% 的阿尔茨海默病是由特定的基因变化引起的,这种基因变化几乎决定了变异者将患上这一疾病。这类人群通常在中年开始发病。
阿尔茨海默病在出现首发症状的几年前就已开始发展。损伤最常始于大脑中负责管理记忆的区域。神经元的丢失以一种大致可以预测的模式扩散到大脑的其他区域。到了疾病后期,大脑已经萎缩。
研究人员试图了解阿尔茨海默病的病因,重点研究两种蛋白质的作用:
- 斑块。 β-淀粉样蛋白是一种较大蛋白质的片段。这些片段聚集在一起,会影响脑细胞之间的通讯。团块会形成较大的沉积物,称为淀粉样蛋白斑块。
- 缠结。 Tau 蛋白在脑细胞的内部支持和运输系统中起着一定的作用,可以运送营养物质和其他必须物质。在阿尔茨海默病患者体内,tau 蛋白会改变形状,形成被称为神经原纤维缠结的结构。这种缠结会破坏运输系统,对细胞造成损伤。
风险因素
阿尔茨海默病的风险因素包括年龄、家族史、生活方式和其他因素。
年龄较大
年龄较大是阿尔茨海默病最强的已知风险因素。阿尔茨海默病并不是正常衰老的一部分。但随着年龄的增长,患这种疾病的几率就会增加。
一项研究发现,每年每 1000 名 65 至 74 岁的老年人中有 4 例新确诊病例。每 1000 名 75 至 84 岁的老年人中有 32 例新确诊病例。每 1000 名 85 岁以上的老年人中有 76 例新确诊病例。
家族史和遗传
如果您的一级亲属(例如父母或兄弟姐妹)被诊断为阿尔茨海默病,则您的患该疾病的风险较高。家族中的基因如何影响风险在很大程度上尚不清楚。遗传因素很可能是复杂的。
得到较多了解的一个遗传因素是载脂蛋白 E(APOE)的一种基因分型。称为 APOE e4 的基因分型会增加患阿尔茨海默病的风险。APOE e4 携带者大约占人口的 25% 到 30%。但并非每个携带这种基因分型的人都会患病。有两个 APOE e4 拷贝的人患阿尔茨海默病的风险会高于有一个拷贝的人。
科学家们在三种基因中发现了罕见变化,几乎可以确定人们遗传其中一种就会患上阿尔茨海默病。但是这些变化在阿尔茨海默病患者中所占比例不足 1%。
唐氏综合征
很多唐氏综合征患者会发展出阿尔茨海默病。这可能与 3 个 21 号染色体拷贝有关,而 21 号染色体基因会参与生成形成 β 淀粉样蛋白的蛋白质。β 淀粉样蛋白片段可能会成为大脑中的斑块。唐氏综合征患者的症状往往比一般人群早出现 10 到 20 年。
出生指定性别
总体而言,女性患者稍多一些,因为她们的寿命通常比男性更长。
轻度认知损害
有些轻度认知损害(也称为 MCI)患者的记忆力或其他思维能力下降的严重程度高于同龄人的正常水平,但这种下降不会妨碍患者的工作或社交功能。
然而,MCI 患者患失智的风险高于没有轻度认知损害者。如果 MCI 主要影响记忆力,由于阿尔茨海默病的影响,该状况更有可能进展为失智。诊断出 MCI 会给患者带来机会,使其关注健康的生活方式变化,针对记忆丧失制定相关弥补策略。患者还可以定期安排医疗护理就诊,以监测症状。
头部受伤
几项大型研究发现,50 岁或以上患有创伤性脑损伤(也称为 TBI)的患者患失智和阿尔茨海默病的风险较高。严重 TBI 和多发性 TBI 患者的风险甚至更高。
空气污染
动物研究发现,空气污染微粒会加速神经系统衰竭。人类研究发现,暴露于空气污染,尤其是交通尾气和木材燃烧产生的污染物,会增加患失智的风险。
酗酒
人们早已知道,大量饮酒会导致脑部发生变化。多项大型研究和综述发现,酒精误用与患失智症风险增加有关,尤其是早发性失智症。
糟糕的睡眠模式
研究表明,不良的睡眠模式,如入睡困难或难以保持睡眠状态,与阿尔茨海默病风险增加有关。睡眠呼吸暂停也可能会增加患失智症的风险。
生活方式和心脏健康
研究表明,导致心脏病的相同风险因素也可能增加患失智的风险。目前尚不清楚这些因素是通过加重脑内阿尔茨海默病变化还是通过导致脑血管变化来增加患病风险。这些因素包括:
- 缺乏运动。
- 肥胖症。
- 抽烟或暴露于二手烟。
- 高血压。
- 高胆固醇。
- 2 型糖尿病管理不佳。
中年时期高水平的低密度脂蛋白(称为 LDL 胆固醇)尤其会增加失智风险。研究发现,LDL 胆固醇水平较高的 65 岁以下人群发生失智的风险较高。但服用降低 LDL 胆固醇的药物不会增加该风险。
这些因素都可以改变,因此改变生活方式可以在一定程度上改变您的风险。例如,坚持定期运动和保持富含果蔬的健康低脂饮食可降低患阿尔茨海默病的风险。
听力减退
研究发现,听力减退的人有患失智症的风险。听力减退越严重,这种风险越高。不过,佩戴助听器可以预防失智症。
未得到治疗的视力减退
最新研究表明,未得到治疗的视力减退是认知损害和失智的一个风险因素。这种联系可能是由于糖尿病等疾病可增加视力减退和失智的风险。但也有研究表明,视力减退本身也可能增加失智的风险。
终生学习和参与社会活动
研究发现,在生活中进行社交和参加能够激励思维的活动可以降低患阿尔茨海默病的风险。教育水平低(高中以下学历)似乎是阿尔茨海默病的一个风险因素。
并发症
阿尔茨海默病可能会导致多种并发症。记忆丧失、语言丧失、判断力受损以及其他脑部变化等症状会使其他健康状况更难管理。阿尔茨海默病患者可能无法:
- 向他人诉说自己的疼痛。
- 说明另一种疾病的症状。
- 遵循治疗计划。
- 说明药物的副作用。
随着阿尔茨海默病进入到晚期,脑部变化开始影响躯体功能。这些变化可能会影响吞咽、平衡以及大小便的控制能力。这些影响可能会导致其他健康问题,例如:
- 肺部吸入食物或液体。
- 流感、感染性肺炎和其他感染。
- 跌倒。
- 骨折。
- 褥疮。
- 营养不良和脱水。
- 便秘或腹泻。
预防
阿尔茨海默病无法预防。但是改变生活方式可以降低患病的风险。
研究显示,采取降低患心血管疾病风险的措施也可能降低患失智的风险。以下有益心脏健康的生活方式可降低患失智的风险:
- 规律运动。
- 采用以新鲜农产品、健康油脂为主且饱和脂肪含量低的饮食,例如地中海饮食。
- 与医疗护理专业人员合作管理高血压、糖尿病和高胆固醇。特别注意您的低密度脂蛋白(称为 LDL 胆固醇)水平。在 65 岁以下人群中,高水平 LDL 胆固醇会增加患失智的风险。但服用降低 LDL 胆固醇的药物不会增加该风险。
- 如果您抽烟,请向医疗护理专业人员寻求戒烟帮助。
在芬兰进行的一项大型长期研究发现,改变生活方式有助于减轻存在患失智风险人群的认知能力下降。研究参加者接受个人和小组治疗,重点是饮食、锻炼和社交活动。
几项研究发现,随着年龄的增长,地中海饮食可维持更好的认知功能,并减缓随着年龄的增长而出现的认知能力下降。地中海饮食以植物性食物为主,例如水果、蔬菜、全谷物、鱼类、家禽、坚果和橄榄油。饮食中应减少饱和脂肪和反式脂肪含量较高的食物,例如黄油、人造黄油、奶酪、红肉、油炸食品和甜点。
治疗视力减退和听力减退也很重要。研究发现,未经治疗的视力减退是患认知损害和失智的风险因素。研究还发现,出现听力减退的人患失智的风险更高。但佩戴助听器会降低人们患失智的可能性。
其他研究表明,保持精神和社交活跃有助于在以后的生活中保持思维能力并降低患阿尔茨海默病的风险。这包括参加社交活动、阅读、跳舞、棋盘游戏、艺术创作、演奏乐器以及其他活动。